JAV Maisto ir vaistų administracija (FDA) papildė Pfizer-BioNTech vakcinos registraciją COVID-19 profilaktikai skubiam vartojimui 5–11 metų amžiaus vaikams. JAV Ligų kontrolės centro (CDC) duomenimis, dėl COVID-19 buvo hospitalizuoti maždaug 8,3 tūkst. vaikų nuo 5 iki 11 metų amžiaus. Spalio 17 d. duomenimis, JAV (330 mln. gyventojų) užregistruotas 691 mirties nuo COVID-19 atvejis jaunesniems kaip 18 metų asmenims, iš jų 146 atvejai – 5–11 metų amžiaus asmenimis. Palyginimui – Lietuvoje yra maždaug 120 kartų mažiau gyventojų, o mirties nuo COVID-19 atvejų jaunesniems kaip 18 metų asmenims neužfiksuota.
Pfizer-BioNTech vakcinos veiksmingumas grindžiamas JAV, Suomijoje, Lenkijoje ir Ispanijoje tęsiamo (dar nebaigto) atsitiktinių imčių placebu kontroliuojamo tyrimo duomenimis. FDA atliko preliminarią COVID-19 atvejų, pasireiškusių praėjus septynioms dienoms po antrosios dozės, analizę, į kurią buvo įtraukti anksčiau SARS-CoV-2 nesirgę tiriamieji. COVID-19 atvejai pasireiškė 3 iš 1 305 paskiepytų ir 16 iš 663 placebą gavusių tirtų asmenų. Apskaičiuota santykinė rizika susirgti COVID-19 paskiepytiems buvo 0,23 proc., o nepaskiepytiems – 2,41 proc., santykinės rizikos sumažėjimas (vakcinos veiksmingumas) – (2,41 % – 0,23 %) / 2,41 % = 90,7 %.
Taigi, pagrindinis klinikinis tyrimas parodė, jog norint apsaugoti 1 vaiką nuo ligos, kurios simptomai dažniausiai būna lengvi, reikėjo paskiepyti daugiau kaip 40.
FDA modeliavimo duomenimis, norint išvengti 1 vaiko hospitalizacijos, reikia paskiepyti maždaug 3 000–5 000 vaikų, o norint išvengti 1 vaiko pateikimo į intensyviosios pagalbos skyrių – maždaug 15 000–20 000 vaikų.
Vis dėlto praktikoje tokiam rezultatui pasiekti gali reikėti paskiepyti dar daugiau, nes nemaža dalis vaikų jau persirgo, o naudos persirgusiems pagrindinis klinikinių tyrimas neįrodė, aiški yra tik rizika.
Be to, labai dažnais atvejais po skiepo vaikai patyrė nesunkių, bet nemalonių trumpalaikių sveikatos sutrikimų. Saugumo duomenys, kuriais grindžiama skubi registracija, buvo gauti stebėjus 3 100 paskiepytų ir 1 538 placebą gavusius 5–11 metų tiriamuosius, iš jų 1 444 buvo stebimi dėl saugumo bent 2 mėnesius po antrosios dozės.
Tokių duomenų nepakanka pastebėti ilgalaikį ir retą šalutinį poveikį, pavyzdžiui, pasireiškiantį 1 iš 5 000 tiriamųjų. Kadangi jau žinoma, kad didžiausia miokardito (širdies raumens uždegimo) ir perikardito (širdį supančių audinių uždegimo) rizika po skiepo kyla 12–17 metų berniukams, FDA atliko modeliavimą, siekdama palyginti, kiek hospitalizacijų, hospitalizacijų intensyviosios terapijos skyriuose ir mirčių nuo COVID-19 galėtų padėti išvengti Pfizer-BioNTech vakcina bei kiek tokių atvejų ji galėtų sukelti pati. COVID-19 vakcinų naudos ir rizikos santykis priklauso nuo COVID-19 plitimo, todėl nauda ir rizika įvertinta pagal kelis scenarijus:
- Pagal COVID-19 atvejų skaičių 2021 m. rugsėjo 11 d.
- Pagal COVID-19 atvejų skaičių, artimą neseniai pasiektam Delta varianto maksimumui.
- Pagal COVID-19 atvejų skaičių, artimą mažiausiam užregistruotam 2021 m. birželio mėnesį.
1 lentelė. Pagal modelį prognozuojama nauda ir rizika milijonui 5–11 metų amžiaus vaikų
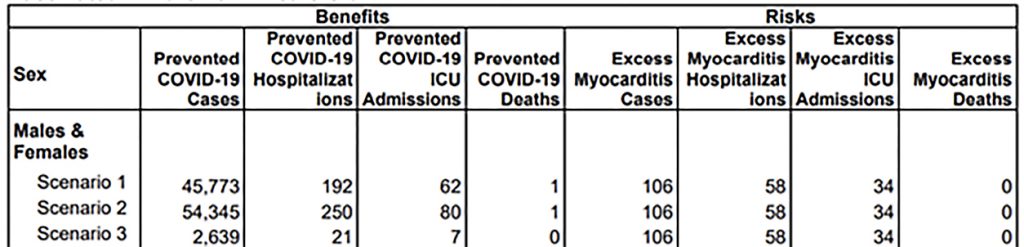
Įvertinus, kad Lietuvoje yra maždaug 200 000 vaikų nuo 5 iki 11 metų, paskiepijus pusę jų idealiu atveju galbūt būtų galima išvengti maždaug 20 hospitalizacijų, iš jų iki 5 – intensyviosios pagalbos skyriuose, t. y. reikia paskiepyti maždaug 20 000 vaikų norint išvengti 1 hospitalizacijos intensyviosios pagalbos skyriuose.
Vis dėlto Sveikatos teisės institutas pažymi, kad:
-
- Šie skaičiavimai yra pagrįsti teorinėmis prielaidomis, padarytomis remiantis hospitalizacijų skaičiumi, tačiau vaikų klinikinis tyrimas, kuriuo remiantis FDA įregistravo vartojimą jiems, sunkios ligos ar hospitalizacijos rizikos sumažėjimo neparodė.
- Trumpalaikio saugumo duomenų yra labai mažai – bent 2 mėnesius stebėti tik 1 444 paskiepyti vaikai. Tokie duomenys negali parodyti retų šalutinių poveikių. Pavyzdžiui, gali būti nepastebėtas labai sunkus ir net mirtinas šalutinis poveikis, kuris pasireikštų 1 iš 2 000 vaikų (jį patirtų atitinkamai 50 vaikų iš 100 000, o tai nusvertų vakcinos naudą). Deja, tokios apimties tyrimai neleidžia įvertinti retų sutrikimų rizikos ir jų ryšio su vakcinacija. Be to, Pfizer-BioNTech vakcinos informaciniuose dokumentuose iki šiol neatspindėtas atvejis, įvykęs 1 iš maždaug 2 000 tiriamųjų 12–15 metų vaikų klinikinio tyrimo metu. Po antrosios vakcinos dozės, suleistos 2021 m. sausio 20 d., 12 metų mergaitei Maddie de Garay pasireiškė stiprus pilvo ir krūtinės skausmas, ji prarado jutimus nuo juosmens žemyn ir pajuto raumenų silpnumą, prarado šlapimo pūslės kontrolę, labai sutriko menstruacijų ciklas ir galiausiai jai buvo įvestas nosies-skrandžio vamzdelis mitybai. Be to, ji negali laisvai judėti.
- Ilgalaikio saugumo duomenų nėra. Turimi duomenys negali parodyti ilgalaikių (pasireiškiančių vėliau kaip po 2 mėnesių) šalutinių poveikių.
Sveikatos teisės institutas ragina Vyriausybę nedaryti skubotų sprendimų. Jeigu Europos vaistų agentūros išvados dėl 5–11 metų vaikų skiepijimo nuo COVID 19 būtų palankios, reikia kruopščiai apsvarstyti, kokiais atvejais gali būti tikslinga siūlyti skiepytis vaikams, išnagrinėjus Europos vaistų agentūros pateiktus argumentus. Skiepijant vaiką būtina įvertinti vakcinos jam duodamą naudą ir keliamą riziką, bet nenaudoti vaikų vakcinacijos procentui padidinti. Būtina atsižvelgti į tai, kad vakcinos naudos ir rizikos santykis persirgusiems neįvertintas, todėl jų skiepijimas būtų nepagrįstas mokslu ir neetiškas. Sprendimą dėl skiepo turi priimti tėvai ir negali būti taikomos jokios diskriminacinės priemonės dėl jų pasirinkimo.
Sveikatos teisės institutas ragina atkreipti dėmesį ir į kitas COVID-19 valdymo priemones, kadangi nors Lietuva paskiepijo didžiausią gyventojų procentą iš 11 pokomunistinių ES valstybių, tačiau COVID-19 laikotarpiu gyventojus apsaugojo beveik blogiausiai iš jų visų (užimą antrą blogiausią vietą tarp šių valstybių pagal mirtingumo padidėjimą).
FDA primena, kad Pfizer ir skiepijimo paslaugų teikėjai PRIVALO pranešti apie visus sunkius nepageidaujamus reiškinius, daugelį sistemų apėmusio uždegiminio sindromo atvejus ir COVID-19 atvejus, dėl kurių paskiepyti asmenys buvo hospitalizuoti arba mirė.
ŠALTINIAI:
- https://www.fda.gov/news-events/press-announcements/fda-authorizes-pfizer-biontech-covid-19-vaccine-emergency-use-children-5-through-11-years-age
- https://www.fda.gov/media/153447/download
- https://www.ema.europa.eu/en/documents/variation-report/comirnaty-h-c-5735-ii-0030-epar-assessment-report-variation_en.pdf
- https://www.youtube.com/watch?v=6mxqC9SiRh8&t=2159s
Visos teisės saugomos ©


